超靈敏電化學發光免疫分析技術 Electrochemiluminescence (ECL)_PD1_MK
美國FDA首個PD-1腫瘤治療藥物-美商默沙東的Keytruda(Pembrolizumab)
美商默沙東公司於2011年開始進行廣泛的使用pembrolizumab治療的人體試驗,第一個第1b期人體試驗(KEYNOTE-001)收錄受試者對象為晚期黑色素瘤及非小細胞型肺癌的患者,並在2014年發表試驗結果,看到顯著延長整體療效反應率以及整體存活率,接著美國食品藥物管理局快速審查通過核准上市,商品名為KEYTRUDA(中譯吉舒達),用以治療罹患無法切除或有轉移現象之黑色素瘤且在使用ipilimumab及BRAF抑制劑(若呈BRAF V600突變陽性)治療後出現疾病惡化現象的患者。於2015年,KEYNOTE-001試驗的非小細胞型肺癌臨床試驗結果發表,顯示若病患的腫瘤細胞有表現PD-1的配體PD-L1,使用吉舒達可顯著延長無惡化期存活率、整體存活率以及整體療效反應率。同年亦獲美國食品藥物管理局核准可用於二線治療腫瘤細胞表現PD-L1的晚期非小細胞型肺癌。吉舒達的作用機轉屬於新一代的藥物,而其研究結果顯示為病患延長存活率以及療效反應率的數據,也使其被一些指標國家的衛生主管機關列入快速審查名單。其藥物代謝及免疫原性、品質控制等項目中使用MSD超靈敏電化學發光免疫分析技術。
Anti PD-1 antibody: Lambrolizumab (MK-3475)
開發藥廠: 美商默沙東公司
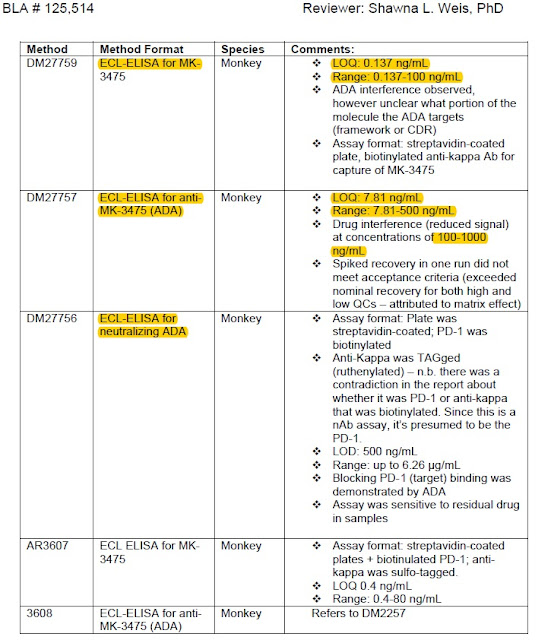
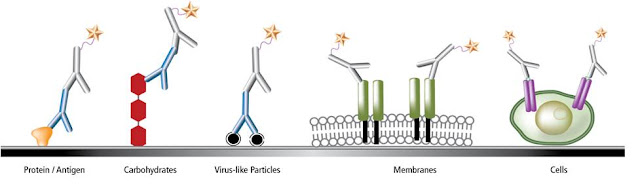
藥物代謝及免疫原性、品質控制等項目方法: ECL ELISA (MSD 超靈敏電化學發光免疫分析技術)







留言
張貼留言